Die Temperatur
Enzyme arbeiten nur in einem bestimmen Temperaturbereich. Dieser ist je nach Enzym variabel. Allgemein gilt erstmal die RGT-Regel. Wird es allerdings zu heiß, kommt es zur Denaturierung. Dass heißt, die Enzyme ändern ihre Konformation, sodass sie ihrer Funktion, dem Katalysieren von biochemischen Reaktionen, nicht mehr nachkommen können.
Bei der Hitzedenaturierung werden die einzelnen Bestandteile (z.B Aminosäuren) so sehr ins Schwingen gebracht, dass Wasserstoffbrückenbindungen, hydrophobe Effekte und Disulfidbrücken zwischen den Bereichen der Molekülkette aufgelöst oder überwunden werden.
Die Hitzedenaturierung kann, sofern die strukturellen Veränderungen nicht zu tiefgreifend sind, reversibel(umkehrbar) sein.
Aufgrunddessen ist auch hohes Fieber ein sehr hohes Risiko für die Gesundheit. Denn durch die hohe Körpertemperatur fangen viele Enzyme an zu denaturieren.
Bei der Hitzedenaturierung werden die einzelnen Bestandteile (z.B Aminosäuren) so sehr ins Schwingen gebracht, dass Wasserstoffbrückenbindungen, hydrophobe Effekte und Disulfidbrücken zwischen den Bereichen der Molekülkette aufgelöst oder überwunden werden.
Die Hitzedenaturierung kann, sofern die strukturellen Veränderungen nicht zu tiefgreifend sind, reversibel(umkehrbar) sein.
Aufgrunddessen ist auch hohes Fieber ein sehr hohes Risiko für die Gesundheit. Denn durch die hohe Körpertemperatur fangen viele Enzyme an zu denaturieren.
Der pH-Wert
Der pH-Wert hat Einfluss auf die Enzymaktivität. Jedes Enzym hat sein eigenes pH-optimum. Bei den meisten Enzymen (Ausnahmen sind beispielweise die Enzyme im Magen) liegt dieses im neutralen Bereich. Bei höheren oder niedrigeren pH-Werten sinkt die Aktivität der Enzyme. Grund dafür ist eine Denaturierung. Zu dieser kommt es, da die Änderung des pH-Wertes Einfluss auf die Ladungsverteilung hat.
Bei der Säuredenaturierung (zu niedriger pH-Wert) beispielsweise gibt die Säure Protonen (H+) ab und verursacht so eine Ladungsänderung in der Aminogruppe (NH2), welche dadurch positiv geladen wird.
Bei der Säuredenaturierung (zu niedriger pH-Wert) beispielsweise gibt die Säure Protonen (H+) ab und verursacht so eine Ladungsänderung in der Aminogruppe (NH2), welche dadurch positiv geladen wird.
Enzymhemmung
Die Enzymaktivität kann beeinflusst werden, wenn andere Stoffe als das eigentlich Substrat an das Enzym binden. Es wird zwischen zwei Arten der Hemmung unterschieden:
|
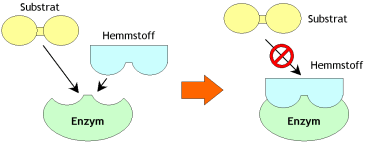
Kompetitive Hemmung:
Substrate binden an Enzyme nach dem Schlüssel-Schloss-Prinzip. Es kann allerdings Stoffe geben, die dem eigentlichen Substrat sehr ähnlich sehen bzw. strukturelle Gemeinsamkeiten aufweisen und aufgrunddessen auch an das aktive/katalytische Zentrum andocken können. Allerdings können diese Stoffe, im Gegensatz zum Substrat, nicht umgesetzt werden. Diese Stoffe blokieren das aktive oder katalytische Zentrum, sodass kein Substrat andocken kann. Die Wirkung solcher Hemmstoffe ist umso größer, je höher die Konzentration im Vergleich zum eigentlichen Substrat ist. Die kompetitive Hemmung kann auch als Verdrängungshemmung bezeichnet werden. Um der Hemmung entgegenzuwirken kann die Substratkonzentration erhöht werden. |
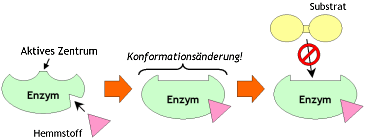
Allosterische Hemmung:
Allosterische Enzyme besitzen, neben dem aktiven oder katalytischen Zentrum ein allosterisches Zentrum. Bindet ein Hemmstoff an das allosterische Zentrum kommt es zu einer Konformationsänderung, welche auch das aktive oder katalytische Zentrum des Enzyms beeinflusst, des Enzyms. Dadurch kann das eigentliche Substrat nicht mehr oder nur sehr schwer an das aktive oder katalytische Zentrum gebunden werden. |
Irreversible Hemmung und Einsatz von Enzymen als Bioindikatoren
Viele Metallionen sind giftig, da sie bei Enzymen eine nicht umkehrbare Konformation bewirken. Besonders giftig sind beispielsweise Quecksilber und Blei, denn diese zerstören die Disulfidbrücken dadurch, dass sie mit Schwefel eine sehr starke Bindung eingehen.
Aufgrund dieser Reaktion auf Schwermetalle können Enzyme als Bioindikatoren eingesetzt werden. So kann man beispielsweise nachweisen, dass schon geringe Mengen von Schwermetallionen die Gäraktivität von Hefezellen beeinflussen. Hefezellen vergären Zucker unter anderem zu Kohlenstoffdioxid. Bringt man eine bestimme Menge der Probe mit Zucker und einer Hefeaufschwemmung zusammen, so zeigt die geringe Entwicklung von Kohlenstoffdioxid eine Belastung der Probe mit Schwermetallionen an.
Aufgrund dieser Reaktion auf Schwermetalle können Enzyme als Bioindikatoren eingesetzt werden. So kann man beispielsweise nachweisen, dass schon geringe Mengen von Schwermetallionen die Gäraktivität von Hefezellen beeinflussen. Hefezellen vergären Zucker unter anderem zu Kohlenstoffdioxid. Bringt man eine bestimme Menge der Probe mit Zucker und einer Hefeaufschwemmung zusammen, so zeigt die geringe Entwicklung von Kohlenstoffdioxid eine Belastung der Probe mit Schwermetallionen an.